
Améliorer l’accès aux médicaments novateurs
Soumission écrite pour les consultations prébudgétaires en vue du budget 2026-2027 du Nouveau-Brunswick
Accédez à une sélection de rapports, de soumissions relatives aux politiques, de données et d’autres documents concernant l’écosystème des sciences de la vie au Canada.

Soumission écrite pour les consultations prébudgétaires en vue du budget 2026-2027 du Nouveau-Brunswick

Médicaments novateurs Canada (MNC) se réjouit de pouvoir contribuer à la réflexion gouvernementale entourant la préparation de son budget 2026-2027. […]

Le marché privé de l’assurance médicaments au Canada a connu une croissance des coûts totaux de 7,3 % en 2023-2024, principalement en raison d’une utilisation accrue qui a représenté 60 % de cette augmentation. Le nombre de réclamants a augmenté de 3,5 %, et leur nombre de réclamations a augmenté de 0,9 %.

Soumission écrite pour les consultations prébudgétaires en vue du prochain budget fédéral

Cette étude examine la contribution du secteur pharmaceutique canadien de la recherche et du développement (R et D) à l’économie canadienne en 2022. Elle s’appuie sur les rapports annuels produits depuis 2018.
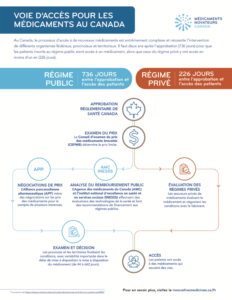
Au Canada, le processus d’accès à de nouveaux médicaments est extrêmement complexe et nécessite l’intervention
de différents organismes fédéraux, provinciaux et territoriaux. Il faut deux ans après l’approbation (736 jours) pour que
les patients inscrits au régime public aient accès à un médicament, alors que ceux du régime privé y ont accès en
moins d’un an (226 jours).
Restez informé en accédant à du contenu d’actualité et pertinent sur le plan des enjeux qui façonnent notre secteur.
